Introducción
La electrodeposición es unatécnica electroquímicacon una historia que abarca más de dos siglos y que implica la deposición de material sobre una superficie conductora mediante la aplicación de corriente eléctrica. Desde sus inicios-desde la primera pila voltaica de Volta en 1800 hasta el descubrimiento de Davy del sodio y el potasio mediante electrólisis en 1807, la electrodeposición ha evolucionado hasta convertirse en unaproceso sofisticadoEsencial en diversas aplicaciones industriales y de investigación. Este método versátil se emplea ahora en campos que van desdeelectrónica y conversión de energíahasta la protección contra la corrosión y la síntesis de materiales catalíticos. El atractivo fundamental de la electrodeposición radica en su capacidad para controlar con precisión el espesor, la composición y la estructura de los materiales depositados, a menudo a temperaturas relativamente bajas y con costos mínimos de equipo en comparación con las técnicas de deposición basadas en el vacío-.
Este artículo proporciona una descripción general completa de la electrodeposición, que cubre susprincipios básicos, los diferentesenfoques tecnológicos, y elmétodos de caracterizaciónSe utiliza para analizar materiales electrodepositados. Ya sea que sea nuevo en el campo o busque profundizar su comprensión, esta guía iluminará la ciencia detrás de esta poderosa técnica de procesamiento de materiales.

1 Principios fundamentales de la electrodeposición
1.1 Conceptos básicos y antecedentes históricos
La electrodeposición es unaproceso electroquímicodonde los iones metálicos en solución se reducen sobre un sustrato conductor bajo la influencia de un campo eléctrico externo. Este proceso ocurre a través de lamigración de ionesen una solución electrolítica hacia electrodos de carga opuesta, donde sufren reacciones de oxidación o reducción.
No se puede subestimar la importancia histórica de la electrodeposición. La técnica ha sido fundamental tanto en descubrimientos científicos fundamentales como en aplicaciones industriales. Su desarrollo a lo largo de más dedoscientos añoslo ha transformado de una curiosidad de laboratorio a un proceso industrial indispensable utilizado en todo el mundo para la síntesis de materiales y la ingeniería de superficies.
1.2 Principio de funcionamiento
En esencia, la electrodeposición se basa enLas leyes de la electrólisis de Faraday., que establecen una relación cuantitativa entre la cantidad de carga eléctrica que pasa a través de un electrolito y la masa de material depositado en los electrodos. La primera ley establece que la masa de sustancia depositada en un electrodo es directamente proporcional a la cantidad de electricidad que pasa a través del circuito. La segunda ley establece que las masas de diferentes sustancias liberadas por la misma cantidad de electricidad son proporcionales a sus pesos equivalentes.
El proceso de electrodeposición ocurre típicamente en uncelda electroquímicaque contiene una solución de electrolitos con sales metálicas disueltas. Cuando se aplica un potencial externo entre dos electrodos, los cationes metálicos (iones cargados positivamente) migran hacia el cátodo (electrodo negativo), donde ganan electrones y se reducen para formar una capa metálica sólida:

DóndeMn+es un ion metálico con n cargas positivas, yMes el átomo de metal neutro incorporado al depósito en crecimiento.
Simultáneamente, en el ánodo (electrodo positivo), se produce la oxidación de los átomos metálicos (en el caso de ánodos solubles) liberando iones metálicos en la solución, o se produce la evolución de oxígeno (en el caso de ánodos inertes).
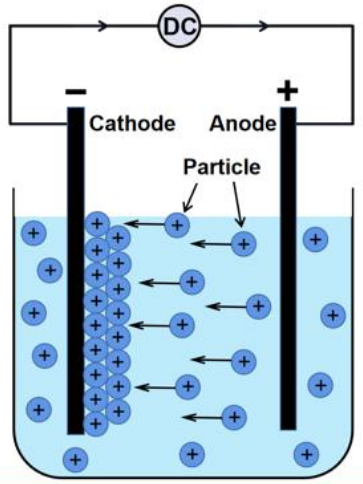
Tabla: Componentes principales en la electrodeposición
| Componente | Función | Ejemplos |
|---|---|---|
| Ánodo | Fuente de iones metálicos o sitio para la evolución de oxígeno. | Cobre, níquel, platino (inerte) |
| Cátodo | Superficie donde ocurre la deposición | Sustratos conductores (metales, semiconductores) |
| Electrólito | Contiene iones metálicos y permite la conducción iónica. | Soluciones acuosas de sales metálicas. |
| Fuente de alimentación | Proporciona energía eléctrica para el proceso. | Fuente de alimentación CC, potenciostato/galvanostato |
1.3 Configuración de electrodos: sistemas de dos-electrodos frente a tres-electrodos
Los sistemas de electrodeposición generalmente se configuran usandodos-electrodootres-electrodoconfiguraciones.
Elsistema de dos-electrodosConsta de un electrodo positivo (ánodo) y un electrodo negativo (cátodo), ambos sumergidos en el electrolito. La fuente de alimentación o estación de trabajo electroquímica proporciona voltaje entre estos dos electrodos. En esta configuración, el voltaje medido representa lavoltaje total de la celdaen toda la celda electroquímica.
Elsistema de tres-electrodoses más avanzado y consta de:
1.Electrodo de trabajo (NOSOTROS): Este es el electrodo donde ocurre la reacción electroquímica de interés (deposición). Sirve como sustrato para la deposición de material.
2.Contraelectrodo (CE): También conocido como electrodo auxiliar, completa el circuito eléctrico y permite que la corriente fluya a través de la celda. Normalmente está hecho de materiales inertes como platino o grafito.
3.Electrodo de referencia (RE): Este electrodo mantiene un potencial estable y conocido contra el cual se puede medir y controlar con precisión el potencial del electrodo de trabajo. Los electrodos de referencia comunes incluyen el electrodo de calomelanos saturados (SCE), el electrodo de Ag/AgCl y el electrodo de Hg/HgO.
En el sistema de tres-electrodos, el electrodo de referencia se coloca cerca del electrodo de trabajo para minimizar los errores debidos a la resistencia de la solución (caída de IR) y las fluctuaciones de voltaje. Este arreglo permitecontrol precisodel potencial del electrodo de trabajo, lo que lo hace preferido para aplicaciones de investigación donde la precisión es crítica.
La configuración de tres-electrodos es particularmente valiosa porque permite a los investigadores controlar con precisión el potencial en el electrodo de trabajo sin interferencias de pérdidas óhmicas o cambios en el contraelectrodo. Esta precisión es esencial para estudios fundamentales de los mecanismos de deposición y para producir depósitos con propiedades específicas.
2 Técnicas de Electrodeposición
Se han desarrollado varios métodos de electrodeposición para satisfacer diferentes requisitos de materiales y necesidades de aplicación. Cada técnica ofrece ventajas únicas en términos de control sobre las propiedades del depósito, eficiencia del procesamiento y aplicabilidad a diferentes sistemas de materiales.
2.1 Electrodeposición convencional

Electrodeposición convencionalAbarca métodos básicos de voltaje constante o corriente constante que forman la base de la tecnología de galvanoplastia. Este enfoque normalmente implica aplicar unacorriente continua continua(DC) entre el ánodo y el cátodo, lo que resulta en una tasa de deposición relativamente constante durante todo el proceso.
La simplicidad de la electrodeposición convencional la hace ampliamente aplicable en entornos industriales para aplicaciones como acabados decorativos, revestimientos-resistentes a la corrosión e interconexiones electrónicas. Sin embargo, ofrececontrol limitadosobre la microestructura del depósito y puede producir depósitos con morfología variable y estructura de grano relativamente gruesa en comparación con técnicas más avanzadas.
2.2 Electrodeposición galvanostática (corriente constante)

Electrodeposición galvanostáticamantiene uncorriente constanteentre el electrodo de trabajo y el contraelectrodo durante el proceso de deposición. La respuesta registrada es el potencial de la celda electroquímica (en un sistema de dos-electrodos) o del electrodo de trabajo (en un sistema de tres-electrodos) en función del tiempo.
A diferencia de la deposición potencial constante, que puede comenzar inmediatamente después de la aplicación potencial, la deposición galvanostática requiere un breve período para iniciarse. Esto se debe a que parte de la corriente aplicada debe cargar primero elcapacitancia de doble capa(Cdl) en la interfaz del electrodo-electrolito. Cuando el potencial alcanza un cierto umbral (normalmente el potencial de equilibrio más el sobrepotencial), comienza la reacción electroquímica.
La corriente constante (I) aplicada consta de dos componentes: Idl (la corriente capacitiva de carga Cdl) e Ict (la corriente de transferencia de carga para la electrodeposición). Cuando comienza la deposición, Idl se acerca rápidamente a cero. La curva potencial-tiempo (curva V-t) obtenida en la deposición galvanostática contiene información esencial sobre los procesos electroquímicos que ocurren durante la deposición.
La principal ventaja de la deposición galvanostática es su capacidad para mantener unatasa de deposición consistente, que es particularmente útil para procesos industriales donde el control del espesor es crítico. Sin embargo, el potencial puede variar durante la deposición, afectando potencialmente las propiedades del depósito si no se controla cuidadosamente.
2.3 Electrodeposición potenciostática (potencial constante)

Electrodeposición potenciostáticaimplica aplicar unpotencial constanteentre los electrodos positivo y negativo (en un sistema de dos-electrodos) o entre los electrodos de trabajo y contraelectrodos (en un sistema de tres-electrodos). La estación de trabajo electroquímica mantiene constante el potencial de deposición y registra la corriente en función del tiempo.
Dependiendo de la relación entre el potencial aplicado y el potencial de equilibrio termodinámico, la deposición potenciostática se puede clasificar en dos regímenes:
1.Deposición de bajo potencial (UPD): Esto ocurre en potenciales por debajo del potencial de equilibrio termodinámico. La UPD implica procesos de adsorción, nucleación y crecimiento determinados por las características de la superficie del sustrato (composición química, estructura cristalina, morfología y humectabilidad del electrolito) y las interacciones del ion-sustrato. Los tipos de cationes y aniones en el electrolito influyen significativamente en la estructura, las propiedades y la cinética de deposición del material depositado.
2.Deposición de sobrepotencial (OPD): Esto ocurre en potenciales por encima del potencial de equilibrio termodinámico. La estructura y las propiedades del OPD dependen en gran medida de varios factores, incluido el sobrepotencial (la diferencia entre los potenciales aplicados y de equilibrio), la concentración de electrolitos, el mecanismo de crecimiento y las interacciones del depósito-sustrato. En particular, la nucleación controlada por difusión-es típicamente el paso-determinante de la velocidad para OPD, mientras que la incorporación de la red en el sustrato es el paso-determinante de la velocidad para UPD.
La principal ventaja de la deposición potenciostática es lacontrol precisosobre la fuerza impulsora de la deposición, lo que permite una mejor manipulación de los procesos de nucleación y crecimiento. Esto a menudo da como resultado depósitos con una morfología más uniforme y una estructura de grano más fina.
2.4 Electrodeposición de Co-
Co-electrodeposiciónes una técnica utilizada para prepararmateriales compuestosoaleacionesdepositando simultáneamente dos o más elementos de la misma solución electrolítica. Este método es particularmente valioso para crear materiales con propiedades mejoradas que no se pueden lograr con depósitos de un solo-elemento.
La co-electrodeposición permite la producción de nanomateriales altamente porosos con áreas superficiales específicas altas, que son valiosas para aplicaciones que requieren una alta actividad electrocatalítica intrínseca. El proceso requiere un control cuidadoso de la composición del electrolito, el pH, la temperatura y los parámetros de deposición para garantizar la co-deposición uniforme de los diferentes elementos con la composición y estructura deseadas.
Esta técnica se utiliza ampliamente para producir depósitos de aleaciones (como latón, bronce o níquel-fósforo) y compuestos de matriz metálica que contienen partículas dispersas de cerámica, polímeros u otros metales.
2.5 Electrodeposición hidrotermal

Electrodeposición hidrotermalcombina la deposición electroquímica contemperatura y presión elevadasCondiciones en un reactor autoclave. Este método es particularmente útil para producir electrocatalizadores conalta cristalinidady estructuras bien-definidas.
El entorno hidrotermal mejora la movilidad de los iones y la cinética de reacción, lo que a menudo da como resultado depósitos con adhesión, densidad y cristalinidad mejoradas en comparación con la electrodeposición a temperatura ambiente. La técnica es especialmente valiosa para depositar óxidos metálicos y otros compuestos que se benefician de las condiciones de síntesis hidrotermal.
Los materiales electrodepositados hidrotermalmente a menudo exhiben una actividad electrocatalítica mejorada debido a sus características estructurales mejoradas, lo que los hace particularmente adecuados para aplicaciones de conversión de energía.
2.6 Electrodeposición asistida por microondas-

Electrodeposición asistida por microondas-utilizaradiación de microondaspara mejorar el proceso de deposición. Esta técnica avanzada puede producir recubrimientos altamente mesoporosos con estructuras únicas que contribuyen a un rendimiento electrocatalítico eficiente.
El campo de microondas interactúa con el electrolito y el depósito en crecimiento a través de varios mecanismos:
Calentamiento dieléctricode la solución, lo que lleva a rápidos aumentos de temperatura
Efectos no-térmicossobre procesos de migración de iones y transferencia de carga
Modificación de la nucleación y crecimiento.cinética
Estos efectos pueden conducir a tasas de deposición aceleradas, estructuras de grano refinadas y características morfológicas únicas que no se pueden lograr fácilmente mediante métodos de electrodeposición convencionales. La electrodeposición asistida por microondas-es particularmente valiosa para crear recubrimientos altamente porosos y de gran-área superficial-para aplicaciones catalíticas y de almacenamiento de energía.
Tabla: Comparación de técnicas de electrodeposición
| Técnica | Parámetro de control clave | Principales ventajas | Aplicaciones típicas |
|---|---|---|---|
| galvanostático | corriente constante | Tasa de deposición controlada, simplicidad | Galvanizado industrial, control de espesor. |
| potenciostático | Potencial constante | Control de potencial preciso, morfología uniforme | Investigación, materiales nanoestructurados. |
| Co-deposición | Múltiples elementos | Materiales compuestos, formación de aleaciones. | Recubrimientos funcionales, catalizadores. |
| hidrotermal | Temperatura/presión | Alta cristalinidad, adhesión mejorada. | Óxidos metálicos, materiales energéticos. |
| Microondas-asistida | Radiación de microondas | Estructuras mesoporosas, morfologías únicas. | Recubrimientos catalíticos, almacenamiento de energía. |
3 Técnicas de Caracterización de Materiales Electrodepositados
La caracterización adecuada de los materiales electrodepositados es esencial para comprender sus propiedades y optimizar los parámetros de deposición. Para este fin se emplean habitualmente varias técnicas analíticas avanzadas.
3.1 Difracción de rayos X-(DRX)

Difracción de rayos X-(DRX)es una potente técnica no-destructiva que se utiliza para analizar laestructura cristalinade materiales electrodepositados. XRD funciona irradiando una muestra con rayos X-y midiendo los ángulos y las intensidades de los haces difractados que emergen.
Cuando los rayos X-interactúan con un material cristalino, se difractan de acuerdo conley de bragg:

Donde λ es la longitud de onda del rayo X-, d es el espacio entre planos atómicos, θ es el ángulo de difracción y n es un número entero.
XRD proporciona información esencial sobre:
Estructura cristalinay composición de fases
Orientación preferida(textura) de cristalitos
Tamaño de cristalitaa través del análisis del ensanchamiento de picos
Parámetros de redy colar
Por ejemplo, en la electrodeposición de películas de Cu₂O sobre vidrio conductor, el análisis XRD reveló que las películas depositadas a 60 grados comenzaron a desarrollar una orientación preferida (111). A medida que aumentó la temperatura del baño, el tamaño de grano de las películas de Cu₂O aumentó de 0,2 μm a 0,4 μm, lo que demuestra cómo la XRD puede rastrear los cambios microestructurales resultantes de diferentes parámetros de deposición.
La XRD es particularmente valiosa para identificar diferentes fases en depósitos de aleaciones o recubrimientos compuestos y para monitorear los cambios estructurales que ocurren durante los tratamientos posteriores-a la deposición, como el recocido.
3.2 Microscopía electrónica de barrido (SEM)

Microscopía electrónica de barrido (SEM)se utiliza para examinar elmorfología de la superficieymicroestructurade materiales electrodepositados a gran aumento. SEM funciona escaneando un haz de electrones enfocado a través de la superficie de la muestra y detectando varias señales generadas por interacciones de electrones-materia.
Las señales principales utilizadas para obtener imágenes en SEM incluyen:
Electrones secundarios (SE): Producido por interacciones inelásticas entre el haz de electrones y los átomos de la muestra, proporcionando contraste topográfico.
Electrones retrodispersados (BSE): Resultado de la dispersión elástica de los electrones incidentes, lo que produce un contraste compositivo basado en diferencias en el número atómico.
SEM proporciona información detallada sobre:
Morfología de la superficiey arquitectura de depósitos
Tamaño de granoy distribución
Porosidady estructura defectuosa
Morfología transversal-y espesor del depósito
Por ejemplo, la caracterización SEM de películas de Cu₂O electrodepositadas reveló unaestructura de superficie similar a una red porosa-. En otro estudio, se utilizó SEM para caracterizar matrices de nanocables de cobre preparadas mediante electrodeposición por pulsos en plantillas de óxido de aluminio anódico (AAO), lo que muestra cómo la intensidad máxima de corriente y los cátodos auxiliares afectaban la calidad de la superficie y la uniformidad de la distribución de longitud.
Los sistemas SEM avanzados pueden incluirespectroscopia de energía-X-dispersiva (EDS)capacidades para el análisis elemental, lo que permite a los investigadores determinar la composición química de los materiales electrodepositados a microescala8.
3.3 Espectroscopía fotoelectrónica de rayos X- (XPS)

Espectroscopía fotoelectrónica de rayos X-(XPS), también conocida como espectroscopía electrónica para análisis químico (ESCA), es una técnica sensible a la superficie-que proporciona información sobre lacomposición químicayestado electronicode elementos en materiales electrodepositados.
XPS funciona basándose en elefecto fotoeléctrico: cuando un material se irradia con rayos X-, los electrones se expulsan de las capas internas de los átomos. La energía cinética de estos fotoelectrones se mide y se relaciona con su energía de enlace mediante la ecuación:
![]()
Donde KE es la energía cinética del electrón expulsado, hν es la energía del fotón de rayos X-, BE es la energía de enlace del electrón y φ es la función de trabajo del espectrómetro.
XPS proporciona información valiosa sobre:
Composición elementalde la superficie (normalmente los 1-10 nm superiores)
Estado químicode elementos (estado de oxidación, ambiente químico)
Uniformidad de composicióna través de la superficie
Espesorde capas superficiales y revestimientos
En el análisis de películas de Cu₂O electrodepositadas, XPS confirmó laalta purezadel material depositado, lo que demuestra la utilidad de la técnica para verificar la composición y pureza del depósito.
XPS es particularmente valioso para analizar películas delgadas y modificaciones de superficies donde el estado químico de los elementos en la superficie influye fuertemente en las propiedades del material. Puede detectar contaminación, estados de oxidación y la eficacia de los tratamientos superficiales.
Tabla: Técnicas de Caracterización de Materiales Electrodepositados
| Técnica | Información obtenida | Profundidad analizada | Consideraciones especiales |
|---|---|---|---|
| XRD | Estructura cristalina, composición de fases, tamaño de grano, textura. | Volumen (μm a mm) | Requiere material cristalino |
| SEM | Morfología superficial, microestructura, espesor. | Superficie a volumen (nm a mm) | Puede requerir revestimiento conductor |
| XPS | Composición elemental, estado químico, estado de oxidación. | Superficie (1-10 nm) | Se requiere un vacío ultra-alto |
4 factores que influyen en la electrodeposición
Varios parámetros influyen significativamente en el proceso de galvanoplastia y en las propiedades de los depósitos resultantes. Comprender y controlar estos factores es esencial para producir materiales con las características deseadas.
Densidad actual(corriente por unidad de área) afecta directamente la tasa de deposición y las propiedades del depósito. Las densidades de corriente más altas generalmente aumentan la tasa de deposición, pero pueden generar depósitos ásperos y porosos con mala adhesión si son excesivamente altas. Los diferentes materiales tienen rangos óptimos de densidad de corriente que producen depósitos densos y suaves.
Elcomposición de electrolitos, incluida la concentración de iones metálicos, el pH y la presencia de aditivos, influyen significativamente en el comportamiento de deposición. A menudo se utilizan aditivos como abrillantadores, niveladores y reductores de tensión-para modificar las propiedades del depósito. La concentración de iones metálicos afecta la densidad de nucleación y el modo de crecimiento.
4.3 Temperatura
Temperaturaafecta la movilidad de los iones, las velocidades de difusión y la cinética de reacción. Las temperaturas más altas generalmente aumentan las tasas de deposición y pueden mejorar la adhesión y densidad de los depósitos. Sin embargo, las temperaturas excesivamente altas pueden provocar una mayor rugosidad y una reducción del poder de lanzamiento (la capacidad de depositarse uniformemente sobre superficies irregulares).
ElpH del electrolitoInfluye en la especiación de iones metálicos y sus potenciales de reducción. Puede afectar la estabilidad de los complejos en la solución, la reacción de desprendimiento de hidrógeno (que compite con la deposición de metales) y las propiedades del material depositado. Mantener el pH adecuado es crucial para obtener resultados consistentes.
5 aplicaciones de la electrodeposición
La electrodeposición encuentra aplicaciones en numerosos campos debido a su versatilidad y rentabilidad-:
Una de las aplicaciones más antiguas y extendidas de la electrodeposición es la producción derevestimientos decorativos y protectores. Los recubrimientos de cromo, níquel, zinc y metales preciosos se utilizan ampliamente en las industrias automotriz, aeroespacial y de bienes de consumo para protección contra la corrosión, resistencia al desgaste y atractivo estético.
En la industria electrónica, la electrodeposición se utiliza para fabricarrastros conductivos, interconecta, ya través de-vías de silicioen dispositivos semiconductores. La electrodeposición de cobre es particularmente importante para la fabricación de circuitos integrados debido a su excelente conductividad eléctrica.
Los materiales electrodepositados desempeñan papeles cruciales entecnologías energéticascomo baterías, pilas de combustible y células solares. La técnica se utiliza para producir electrodos con gran superficie, materiales catalíticos para pilas de combustible y películas delgadas para dispositivos fotovoltaicos.
La electrodeposición puede producirnanoestructuras altamente porosascon grandes superficies, lo que los hace ideales para aplicaciones catalíticas. Materiales como óxidos de metales de transición y metales nobles se pueden depositar como catalizadores eficientes para diversas reacciones químicas, incluida la evolución de hidrógeno, la evolución de oxígeno y las reacciones de reducción de oxígeno.
Conclusión
La electrodeposición es una técnica versátil y poderosa para fabricar materiales funcionales con estructuras y propiedades controladas. Desde sus principios fundamentales basados en reacciones electroquímicas hasta técnicas avanzadas como la deposición hidrotermal y asistida por microondas-, el campo ofrece numerosos enfoques para la síntesis de materiales.
Las técnicas de caracterización analizadas-XRD, SEM y XPS-proporcionan herramientas esenciales para comprender las relaciones entre los parámetros de deposición y las propiedades del material resultante. Este conocimiento permite el diseño racional de materiales electrodepositados para aplicaciones específicas en diversos campos, incluidos la electrónica, la energía, la catálisis y la ingeniería de superficies.
A medida que la investigación siga avanzando, las técnicas de electrodeposición probablemente evolucionarán para permitir un control aún mayor sobre la estructura del material a nanoescala, abriendo nuevas posibilidades para los materiales y dispositivos de próxima-generación. La combinación de comprensión teórica, experiencia experimental y caracterización avanzada hace que la electrodeposición sea una herramienta indispensable en la ciencia e ingeniería de materiales modernas.
